近大-ルイジアナ州立大学 (LSU) 多発性硬化症研究チーム
近大-LSU多発性硬化症研究チーム 研究グループとプログラム
I. 多発性硬化症とは?
II. Kindai-LSU多発性硬化症研究チーム 概要
III. 神経免疫学 グループ
IV. 血管生理学・マイクロ・パーティクル グループ
V. バイオインフォーマティクス・システム生物学グループ
VI. 神経ウイルス学・神経病理学グループ
I. 多発性硬化症とは? 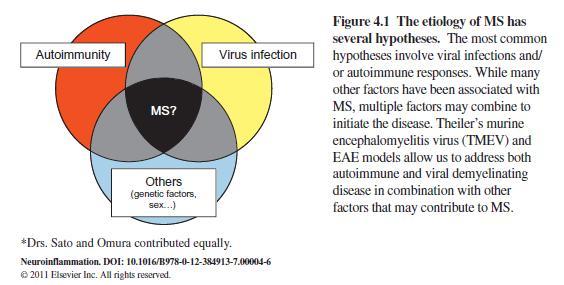
多発性硬化症(Multiple sclerosis、MS)は中枢神経(脳と脊髄 central nervous
system、CNS)の病気で、病理学的には炎症と脱髄がその特徴とされる疾患です。欧米に多い疾患ですが、近年、日本でも患者数が増加しています。原因は現在のところ不明ですが、
自己免疫(autoimmunity 自己の組織を標的として攻撃する免疫反応), 感染症、特ウイルス感染(virus
infections), や遺伝要因(genetic factors)が、その発症に関連があると推察されています (Figure 4.1). 自己免疫説を支持するデータとしては、
多発性硬化症ではミエリン(髄鞘)特異的なT細胞や自己抗体が検出されることや、脱髄を起こしている病変部に免疫細胞が検出されることがあげられます。
また、免疫を調整する薬( Immunomodulatory drugs)であるコパクソン (glatiramer acetate、 copaxone), I型インターフェロン{interferon (IFN)-beta (Avonex, Betaseron, Rebif)},
接着分子VLA-4に対する抗体 {anti-very late antigen (VLA)-4 antibody (Natalizumab, Tysabri)}が再発寛解型の多発性硬化症の治療に有効であることも自己免疫説を支持するデータです。
実験的には動物に自己免疫を導入することで、多発性硬化症類似の病変を再現することができ、これを実験性自己免疫性(アレルギー性)脳脊髄炎{experimental autoimmune
(allergic) encephalomyelitis (EAE)}と呼び、病理学的にも炎症と脱髄が中枢神経に限局して認められることが知られています。
微生物による感染症(Microbial infections),特にウイルス感染も多発性硬化症の原因あるいは増悪因子として推察されています。これを支持するデータ
としては、多発性硬化症の患者さんから採取されたサンプルなどから、ある種のウイルスあるいはウイルスに対する免疫反応が検出されることなどですが、実験的には
動物に特定のウイルスを接種することで、多発性硬化症類似の病変を再現できることが知られています。代表例としては
犬ジステンパーウイルス( canine distemper virus)マウス肝炎ウイルス (murine hepatitis virus)などが挙げられますが、もっとも頻用されているウイルスモデルはタイラーウイルス(TMEV、 Theiler’s murine encephalomyelitis virus)
を用いたもので1975年より使用されています。タイラーウイルスモデルでは、ウイルス自身と免疫細胞の両者が病変形成に重要な働きをしていることが解明されています。
 II. 近大-LSU多発性硬化症研究チーム 概要
II. 近大-LSU多発性硬化症研究チーム 概要
多発性硬化症(Multiple sclerosis、MS)は免疫性神経難病で世界で300万人以上、日本では約1万人、米国ルイジアナ州には約4000人の患者さんがいます。近大ールイジアナ州立大学(Louisiana State University, LSU)多発性硬化症研究チーム(Kindai-LSU MS Research Team)は、複数の研究室からなる
近畿大学とルイジアナ州おける多発性硬化症研究の拠点です。おもな研究室はLSUで血管の生理学を研究するJ スチーブ・アレクサンダー(J Steven Alexander, PhD)教授のグループ、リンパ球の機能や神経細胞の異常を解析する我々のグループ(近畿大学微生物学講座)
,臨床神経学的側面から研究をすすめる神経内科学講座のアリレザ・ミナガー教授(Alireza Minagar, MD)です.
我々は多発性硬化症の一日も早い原因の究明と治療法の開発のために、多発性硬化症関係のボランティア活動にも、積極的に参加しております。そのひとつの例が、 Kindai-LSU多発性硬化症研究チームのシュリーブポート・ボージャー市で行われたチャリテー募金活動である”多発性硬化症行進”  への参加です。
多発性硬化症行進(Walk MS)は米国の多発性硬化症のチャリテー募金運動では最も大きなものです。シュリーブポート・ボージャー市(Shreveport-Bossier City)ではハリケーン カトリーナの襲来後、多発性硬化症行進は途絶えていましたが、
角田研究室の参加などの協力もあり、2011年より再開することができました。角田研究室のメンバーを中心とするルイジアナ州立大学(LSU)の多発性硬化症研究チームは”LSUタイガース”というチャリテーのチームを作成し、毎年、2015年まで、先頭にたって募金活動に協力しました。
”タイガース”という名称は、ルイジアナ州立大学のマスコットの虎にちなんだ名前で、ルイジアナ州立大学のフットボールのチーム名もタイガースとなっています。我々は、今後は、日米で、他のチームに先立って、チームを作成し、市民教育などに携わっていく計画です。
への参加です。
多発性硬化症行進(Walk MS)は米国の多発性硬化症のチャリテー募金運動では最も大きなものです。シュリーブポート・ボージャー市(Shreveport-Bossier City)ではハリケーン カトリーナの襲来後、多発性硬化症行進は途絶えていましたが、
角田研究室の参加などの協力もあり、2011年より再開することができました。角田研究室のメンバーを中心とするルイジアナ州立大学(LSU)の多発性硬化症研究チームは”LSUタイガース”というチャリテーのチームを作成し、毎年、2015年まで、先頭にたって募金活動に協力しました。
”タイガース”という名称は、ルイジアナ州立大学のマスコットの虎にちなんだ名前で、ルイジアナ州立大学のフットボールのチーム名もタイガースとなっています。我々は、今後は、日米で、他のチームに先立って、チームを作成し、市民教育などに携わっていく計画です。
近大微生物学講座のの多発性硬化症研究は、 ルイジアナ州立大学の分子性・腫瘍ウイルス学センター(CMTV)  から、研究費や設備、その他の支援をうけています。
分子性・腫瘍ウイルス学センター(Center for Molecular and Tumor Virology, CMTV)は分子生物学・腫瘍ウイルス学を専門とする独立した複数の研究室が共同研究を円滑に進めることを目的としています。
センターでは、所属するシニア教授陣はジュニアメンバーの教授陣の医学生物研究をサポートするシステムができております。センターはNIHのCOBRE研究費で運営されており、各種の分子生物学的解析サービス、試薬、各種精密機械、
技術面のサポートをすることによって、センターの所属メンバーの研究活動を高めています。CMTVの一環のバイオインフォーマティクス施設 (Bioinformatics Core)は、ルイジアナ州立大学シュリーブポート校にあり、各種のデータ解析、
バイオインフォーマティクス, データマイニング(data mining)を可能にしています。.
から、研究費や設備、その他の支援をうけています。
分子性・腫瘍ウイルス学センター(Center for Molecular and Tumor Virology, CMTV)は分子生物学・腫瘍ウイルス学を専門とする独立した複数の研究室が共同研究を円滑に進めることを目的としています。
センターでは、所属するシニア教授陣はジュニアメンバーの教授陣の医学生物研究をサポートするシステムができております。センターはNIHのCOBRE研究費で運営されており、各種の分子生物学的解析サービス、試薬、各種精密機械、
技術面のサポートをすることによって、センターの所属メンバーの研究活動を高めています。CMTVの一環のバイオインフォーマティクス施設 (Bioinformatics Core)は、ルイジアナ州立大学シュリーブポート校にあり、各種のデータ解析、
バイオインフォーマティクス, データマイニング(data mining)を可能にしています。.
III. 神経免疫学 グループ
角田研究室はリンパ球やマクロファージなどの免疫細胞の中枢神経内での研究である神経免疫学を、その研究の一つの柱にしています。自然抗体、ナチュラル・キラーT細胞、CD8陽性細胞障害性T細胞の多発性硬化症モデルにおける役割を、独自に
研究しているほか、マシュー B. グリシャム 教授との共同研究で制御性T細胞の研究を、高橋智教授との共同研究で、ヘルパーT細胞の研究をしております。
マシュー B. グリシャム 教授 研究室 テキサステック大学医学部免疫学・分子微生物学講座 
マシュー B. グリシャム 教授はテキサス州ラボックのテキサステック大学免疫学・分子微生物学講座のチェアマン・教授で、炎症性腸炎など免疫性疾患の研究に長年携わっています。グリシャム研究室は制御性T細胞 (regulatory T cell, Treg)の新しい
誘導法を開発し、自己免疫病の治療方法への応用を検討しています。角田研究室は、このグリシャム教室の開発した誘導性Treg (iTreg)細胞が多発性硬化症をはじめとする免疫性疾患の治療への適用を共同研究しています。
高橋智教授 解剖学発生学研究室 筑波大学大学院人間総合科学研究科生命システム医学専攻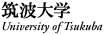
個体の疾患感受性は,免疫系の制御を司るT細胞のサブセットバランスにより決定されています.T細胞サブセットはT helper (Th)1,Th2,TH17およびregulatory T (Treg)に分画され,それらの細胞の形成には T-bet, Gata-3, c-Maf, RORγtおよびFoxp3が重要です。
高橋智教授の研究室は、これまで、疾患感受性決定に対するT細胞サブセットの機能をそれらの転写因子を中心に解析しています。角田研究室は、高橋教授と筑波大学腎臓内科の楊景堯准教授らの開発したトランスジェニックを用いて、Th1,Th2, Th17細胞の多発性硬化症モデルにおける役割を研究しております。
高橋智教授は東北大学医学部の先輩でもあり、2011年に筑波大学にて角田郁生による: 第330回つくば分子生命科学セミナー
“多発性硬化症自己免疫モデルとウイルスモデルの軸索変性に対する赤ワイン成分の一つであるレスベラトロールの効果”を主催していただきました. (写真).
IV. 血管生理学・マイクロ・パーティクル グループ
角田研究室が最も緊密に共同研究を行っているのが、アレクサンダー教授とミナガー教授のグループです。合同グループミーティングなどを頻繁に行い情報交換と技術協力をし、これまで複数のプロジェクトで成果をあげ、国内外の学会で発表を行い、論文や総説を共同で発表しております。
J. スティーブ・アレクサンダー 教授 研究室 ルイジアナ州立大学医学部生理学講座 
アレクサンダー教授研究室では小血管・リンパ管の炎症病変や神経病変における変化を研究しています。対象としている病気は多岐にわたり、多発性硬化症、脳卒中、アルツハイマー病、がん、クローン病、糖尿病 などです。角田研究室とは多発性硬化症
の共同研究をすすめてきましたが、最近では心筋炎のモデルでも共同研究を行っています。
アリレザ・ミナガー教授 研究室 ルイジアナ州立大学医学部神経内科学講座 
アリレザ・ミナガー教授は、神経内科認定医で、神経免疫学とくに多発性硬化症を専門にしています。ミナガー教授は多発性硬化症の免疫調整剤の治験の臨床研究に携わる傍ら、角田研究室やアレクサンダー研究室と共同研究を行い、脳血管とリンパ球の相互作用、リンパ球の組織内浸潤、
血管内皮細胞のマイクロパーティクルの多発性硬化症における役割の解明に取り組んでいます。また、多発性硬化症の臨床型の予想や免疫調整剤の反応の結果の判定に役立つバイオマーカーの発見にも取り組んでいます。
V. バイオインフォーマティクス・システム生物学グループ
近大微生物学講座では、次世代シークエンス、マイクロアレイやその他の手法を用いて得られた膨大な実験データを、バイオインフォーマティクス・システム生物学の手法を駆使して解析しています。解析にあたっては、ルイジアナ州立大学シュリーブポート校コンピュータ講座のトラッチェル
教授とシビック教授と共同研究をしており、主成分分析やパスウェイ解析など多様な方法により、データマイニングを行っています。
Dr. Marjan Trutschl 研究室 コンピュータ・サイエンス講座 ルイジアナ州立大学 シュリーブポート校 
マリヤン・トラッチェル(Marjan Trutschl)博士はルイジアナ州立大学シュリーブポート校のコンピュータ サイエンス講座で研究室を主催しており、角田研究室とはバイオインフォーマティクスの手法を用いた膨大かつ複雑な実験データの解析を
スーパーコンピュータなどを駆使して行い共同研究を進めています。
Dr. Urska Cvek 研究室 コンピュータ・サイエンス講座 ルイジアナ州立大学 シュリーブポート校 
ウルスカ・シビック教授の研究室はシステム生物学的手法でマイクロアレイをはじめとする膨大かつ多様なデータの解析を角田研究室と共同で行っています。”R”や”Significance Analysis of Microarrays (SAM)
"などの統計ソフトを使い主成分分析(principal component analysis, PCA)を含む解析方法で多発性硬化症のバイオマーカーの発見や、個々の患者さんごとのテーラーメードの治療法(Personalized Medicine)の選択をめざし、実験データが臨床に反映されるような橋渡し研究(トランスレーショナルリサーチ,Translational Research)を行っています。,
Dr. John A. Vanchiere 研究室 ルイジアナ州立大学医学部 小児科学講座 
ジョン・バンチリー教授の研究室は、単一の生体サンプルで、サイトカインやケモカインを含むの複数のタンパク質の同時“マルチプレックス“解析をおこなう技術を駆使して、患者血清などの解析を行っています。角田研究室との共同研究では、Luminex xMAPマルチプレックス技術を利用したシステムを用いています。これは、蛍光標識ビーズの表面上で多様なバイオアッセイを行い、単一試料の試験における時間、労力とコストを低減するものです。
xMAPテクノロジーは、従来型のELISAやウェスタンブロッティングなどの個々のタンパク質を検出する方法と比べると、生体サンプルからタンパク質を「マルチプレックス(複数のアナライトを同時に)」 検出する画期的な技術と言えます。
現在は、わずか25μLのサンプルで32種類のサイトカインとケモカインを同時に測定するMouse Cytokine/Chemokine Magnetic Bead Panelなどを使用しています。
VI. 神経ウイルス学・神経病理学グループ
 近大微生物学講座では、多発性硬化症のウイルスモデルであるタイラーウイルスを使用して、ウイルスの中枢神経内における役割をこれまで解明していきました(神経ウイルス学)。また、病理学の手法を用いて、中枢神経内でどのような病理学的変化が、多発性
硬化症モデルにおいて起こっているのかを解明してきました(神経病理学)。
近大微生物学講座では、多発性硬化症のウイルスモデルであるタイラーウイルスを使用して、ウイルスの中枢神経内における役割をこれまで解明していきました(神経ウイルス学)。また、病理学の手法を用いて、中枢神経内でどのような病理学的変化が、多発性
硬化症モデルにおいて起こっているのかを解明してきました(神経病理学)。
多発性硬化症における神経病理は脱髄が特徴的で、神経の軸索は保存されるとされてきましたが、近年軸索も早期より障害されることが明らかになってきました。
軸索障害の原因は明らかではありませんが、これまで主流である説は、障害の対象はミエリン {myelin (myelinopathy)}か、あるいはミエリン形成細胞である乏突起膠細胞 {オリゴデンドロサイト
oligodendrocytes (oligodendrogliopathy)}であり、ミエリンに包まれている軸索は、ミエリンの障害によって二次的に変性するというものです。
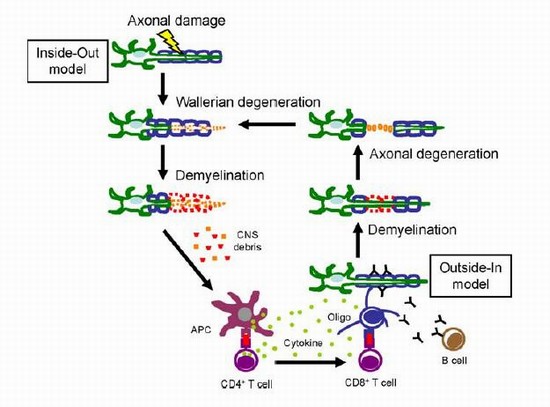
この仮説では、たとえばミエリンに対する自己免疫反応がまず、神経線維の外側を覆っているミエリンを攻撃し障害を与え脱髄病変を生じます。ここにおいて、ミエリンがなくなってしまってむき出しになった軸索は、炎症が継続すれば障害されるというわけです。
病変が外側のミエリンから内側の軸索へと進むので、これをアウトサイドーイン モデル“Outside-In” modelと呼称されています。
ところが、病理学的検索や放射線学的検索(MRIやMRSなどの画像診断)によると、多発性硬化症の病変によっては、軸索変性が脱髄病変のないところに生じているのが見つかったりすることから、すべての
病変を、このアウトサイドーイン モデルで説明することは難しいことがわかってきました。
実際、ウイルスモデルのタイラーウイルス感染症や犬ジステンパーウイルスモデルでは軸索障害が脱髄に先行しておこることが解っております。また、自己免疫モデルのEAEでも
動物を軸索に対する抗原など{neurofilament light protein、contactin-2/transiently expressed axonal glycoprotein 1 (TAG-1)}
で免疫すると軸索障害が先行する多発性硬化症類似の病変が生ずることが知られています。この場合は病変が内側の軸索から外側のミエリンへと進展しますので、これは
インサイドーアウト モデル “Inside-Out” modelと呼称されています。. この仮説においてまず軸索が傷害され、これがオリゴデンドロサイトのアポトーシスを誘導し、二次的に脱髄にいたるというのが一つの提唱されている機序です。
ここで強調したいのは、上記の二つのモデルは矛盾するものではなく、お互いに増強しあい悪循環を生じるものであるという点です。脱髄なり軸索変性が起こりますと、脳のマクロファージであるミクログリアが
活性化され、変性したミエリンや軸索を貪食し、これをT細胞などの免疫細胞に抗原提示することができます。これによって、神経組織に対する自己免疫反応が誘導あるいは増強されますので、病変が外側から始まろうと
内側から始まろうと、炎症反応は増強していくことになります。我々は、これが多発性硬化症の病気の進行に関与していると仮説を建てております。
レーザーマイクロダイセクション (LCM) 施設 ルイジアナ州立大学医学部 
レーザーマイクロダイセクション (Laser capture microdissection, LCM)は組織切片から個々の細胞を切り取って解析を可能にする方法です。切り取ってきた細胞からはDNAやRNAを抽出し、遺伝子発現の解析をすることができます。
レーザーマイクロダイセクション法では、レーザーを使うことによって組織内の特定部分からサンプルを採取いたします。 角田研究室は、ルイジアナ州立大学医学部のLCM施設において、LCMの専門家である ル・ジャン (Ru Jiang)博士 (微生物学・免疫学講座
, ハット・フレッチャー(Hutt-Fletcher)研究室)との共同研究で多発性硬化症サンプルなどの解析を進めています。
PDF and reprint request Information:
住所:
〒590-0197 近畿大学医学部微生物学講座
大阪府堺市南区三原台1丁14番1号
Eメール: itsunoda@hotmail.com または itsunoda@med.kindai.ac.jp
電話: 072-288-7222 (ext. 5040, or 2054), or 072-288-7350
ファックス: 072-298-1500

 II. 近大-LSU多発性硬化症研究チーム 概要
II. 近大-LSU多発性硬化症研究チーム 概要
 への参加です。
多発性硬化症行進(Walk MS)は米国の多発性硬化症のチャリテー募金運動では最も大きなものです。シュリーブポート・ボージャー市(Shreveport-Bossier City)ではハリケーン カトリーナの襲来後、多発性硬化症行進は途絶えていましたが、
角田研究室の参加などの協力もあり、2011年より再開することができました。角田研究室のメンバーを中心とするルイジアナ州立大学(LSU)の多発性硬化症研究チームは”LSUタイガース”というチャリテーのチームを作成し、毎年、2015年まで、先頭にたって募金活動に協力しました。
”タイガース”という名称は、ルイジアナ州立大学のマスコットの虎にちなんだ名前で、ルイジアナ州立大学のフットボールのチーム名もタイガースとなっています。我々は、今後は、日米で、他のチームに先立って、チームを作成し、市民教育などに携わっていく計画です。
への参加です。
多発性硬化症行進(Walk MS)は米国の多発性硬化症のチャリテー募金運動では最も大きなものです。シュリーブポート・ボージャー市(Shreveport-Bossier City)ではハリケーン カトリーナの襲来後、多発性硬化症行進は途絶えていましたが、
角田研究室の参加などの協力もあり、2011年より再開することができました。角田研究室のメンバーを中心とするルイジアナ州立大学(LSU)の多発性硬化症研究チームは”LSUタイガース”というチャリテーのチームを作成し、毎年、2015年まで、先頭にたって募金活動に協力しました。
”タイガース”という名称は、ルイジアナ州立大学のマスコットの虎にちなんだ名前で、ルイジアナ州立大学のフットボールのチーム名もタイガースとなっています。我々は、今後は、日米で、他のチームに先立って、チームを作成し、市民教育などに携わっていく計画です。  から、研究費や設備、その他の支援をうけています。
分子性・腫瘍ウイルス学センター(Center for Molecular and Tumor Virology, CMTV)は分子生物学・腫瘍ウイルス学を専門とする独立した複数の研究室が共同研究を円滑に進めることを目的としています。
センターでは、所属するシニア教授陣はジュニアメンバーの教授陣の医学生物研究をサポートするシステムができております。センターはNIHのCOBRE研究費で運営されており、各種の分子生物学的解析サービス、試薬、各種精密機械、
技術面のサポートをすることによって、センターの所属メンバーの研究活動を高めています。CMTVの一環のバイオインフォーマティクス施設 (Bioinformatics Core)は、ルイジアナ州立大学シュリーブポート校にあり、各種のデータ解析、
バイオインフォーマティクス, データマイニング(data mining)を可能にしています。.
から、研究費や設備、その他の支援をうけています。
分子性・腫瘍ウイルス学センター(Center for Molecular and Tumor Virology, CMTV)は分子生物学・腫瘍ウイルス学を専門とする独立した複数の研究室が共同研究を円滑に進めることを目的としています。
センターでは、所属するシニア教授陣はジュニアメンバーの教授陣の医学生物研究をサポートするシステムができております。センターはNIHのCOBRE研究費で運営されており、各種の分子生物学的解析サービス、試薬、各種精密機械、
技術面のサポートをすることによって、センターの所属メンバーの研究活動を高めています。CMTVの一環のバイオインフォーマティクス施設 (Bioinformatics Core)は、ルイジアナ州立大学シュリーブポート校にあり、各種のデータ解析、
バイオインフォーマティクス, データマイニング(data mining)を可能にしています。.







 近大微生物学講座では、多発性硬化症のウイルスモデルであるタイラーウイルスを使用して、ウイルスの中枢神経内における役割をこれまで解明していきました(神経ウイルス学)。また、病理学の手法を用いて、中枢神経内でどのような病理学的変化が、多発性
硬化症モデルにおいて起こっているのかを解明してきました(神経病理学)。
近大微生物学講座では、多発性硬化症のウイルスモデルであるタイラーウイルスを使用して、ウイルスの中枢神経内における役割をこれまで解明していきました(神経ウイルス学)。また、病理学の手法を用いて、中枢神経内でどのような病理学的変化が、多発性
硬化症モデルにおいて起こっているのかを解明してきました(神経病理学)。